蛹虫草Cordyceps militaris (L.) Link又名北虫草,隶属于子囊菌门Ascomycota、粪壳菌纲Sordariomycetes、肉座菌目Hypocreales、虫草菌科Cordycipitaceae、虫草属Cordyceps(梁宗琦2007)。蛹虫草不仅营养丰富,还富含多种活性物质,如虫草素、N6-(2-羟乙基)腺苷、虫草酸、虫草多糖、类胡萝卜素等,具有抗肿瘤、抗衰老、抗病毒、调节免疫力等功效(贾国军等2017;Yan et al. 2020)。随着人民保健意识的增强,对保健食品的需求日益增长,促进了蛹虫草产业的迅速发展,目前规模化人工栽培及其深加工产业已初步形成。据中国食用菌协会统计,2018年我国蛹虫草年产量已达到9万多吨,产值达100多亿人民币(刘晴等2021)。蛹虫草在栽培过程中普遍存在菌种退化、产量降低或不能正常出草等问题,成为其产业化发展的主要瓶颈,选育高产优质菌株并确立优良菌种的分离提纯方法,成为蛹虫草产业发展亟待解决的关键技术问题。
野生蛹虫草分布广泛且遗传多样性丰富,是新品种选育中一类重要的种质资源。目前蛹虫草纯菌种的获得仍借鉴担子菌的经验技术,以组织分离为主。近些年研究发现,不同部位分离的虫草菌株在菌丝长势和出草性状方面均存在显著差异(袁源等2021;肇莹等 2021;周绍琴等2021),如杨玉红等(2012)发现从靠近子座顶端分离的菌种易于萌发,而子囊孢子分离得到的菌株出草性状更好;郭俊霞等(2015)通过对不同部位分离菌株的成活率、污染率、菌丝长势方面比较得出,靠近子座顶端分离的菌株要优于分离自子座下部的菌株;吕延华等(2016)从西藏新鲜冬虫夏草不同部位分离菌株,并进行固体培养,通过比较分离自冬虫夏草不同部位的菌株的菌丝生长、分生孢子产生情况及不同传代次数菌株的固体培养特性得出,子囊孢子分离获得的菌株在菌丝长势、出草能力和分生孢子产生量等方面显著高于组织分离菌株,而同为组织分离的菌株中,以子座来源的菌株产孢能力显著高于菌核来源的菌株。目前关于该方面的研究较少,且主要停留在菌丝长势和产量方面,关于不同部位分离菌株间营养成分差异等方面的研究较少。因此,立足各地野生蛹虫草资源,对从不同样本、不同部位分离获取菌株的综合性状开展评价分析,对蛹虫草优良菌株的选育和优良菌种的分离提纯具有指导意义。
基于此,本研究对分离自泰山地区6株野生蛹虫草标本不同部位(子座、菌核和子囊孢子)18个菌株的菌丝长势、出草特性及活性物质含量等方面开展综合评价,并对其交配型基因进行鉴定,探究不同野生型菌株、同一菌株不同分离部位的菌株间综合性状差异,以期为今后野生蛹虫草资源的开发利用提供理论依据。
1 材料与方法
1.1 材料
1.1.1 供试菌株:本实验以采集分离自泰山地区(117°7’9’’E,36°20’6’’N,海拔750-850m)的6株野生蛹虫草子实体作为实验材料,分别通过子座、菌核组织分离和子囊孢子分离得到18个菌株,编号见表1,经鉴定均为蛹虫草菌株,现保藏于山东农业大学菌物实训实践基地实验室。
表1 菌株编号
Table 1
| 分离部位 Separating part | F1 Natural sample F1 | F2 Natural sample F2 | F3 Natural sample F4 | F4 Natural sample F4 | F5 Natural sample F6 | F6 Natural sample F6 |
|---|---|---|---|---|---|---|
| 菌核 Sclerotium | F1-1 Isolated from F1 sclerotium | F2-1 Isolated from F2 sclerotium | F3-1 Isolated from F3 sclerotium | F4-1 Isolated from F4 sclerotium | F5-1 Isolated from F5 sclerotium | F6-1 Isolated from F6 sclerotium |
| 子座 Stroma | F1-2 Isolated from F1 stroma | F2-2 Isolated from F2 stroma | F3-2 Isolated from F3 stroma | F4-2 Isolated from F4 stroma | F5-2 Isolated from F5 stroma | F6-2 Isolated from F6 stroma |
| 子囊孢子 Ascospore | F1-3 Isolated from F1 ascospore | F2-3 Isolated from F2 ascospore | F3-3 Isolated from F3 ascospore | F4-3 Isolated from F4 ascospore | F5-3 Isolated from F5 ascospore | F6-3 Isolated from F6 ascospore |
1.1.2 培养基:PPDA培养基:马铃薯200g,葡萄糖20g,蛋白胨10g,琼脂18g,磷酸二氢钾1.5g,硫酸镁0.5g,VB1 0.1g,去离子水1 000mL,pH自然。液体培养基:马铃薯200g,葡萄糖20g,蛋白胨10g,磷酸二氢钾1.5g,硫酸镁0.5g,VB1 0.1g,去离子水1 000mL,pH自然。出草培养基:大米38g,蚕蛹粉2g,营养液60mL(配方同液体菌种培养基)。水琼脂培养基:去离子水1 000mL,琼脂粉16g。
1.2 方法
1.2.1 菌株分离:(1)菌核分离:用灭菌手术刀剥开蛹体,用镊子挑取内菌核组织块接种至PPDA培养基,待菌丝萌发后及时转移至新的PPDA培养基上进行纯化。(2)子座分离:用灭菌手术刀切取蛹虫草子座顶端1cm大小子实体段,放入30%过氧化氢中漂洗20-30s,转移至无菌水中漂洗30s,灭菌滤纸吸干子实体表面水分后用手术刀将子实体剥开,从中挑取一小块子实体接种至PPDA培养基,待菌丝萌发后及时转移至新的PPDA培养基上进行纯化。(3)孢子分离:取子实体可孕部1-1.5cm,放入30%过氧化氢中漂洗20-30s,转移至无菌水中漂洗30s,用灭菌滤纸吸干子实体表面水分后用细线将其绑住,悬挂于制备好的水琼脂培养基的正上方,22-23℃下过夜后,取出虫草子实体继续培养,待孢子萌发后立即转移至PPDA培养基上进行培养。
1.2.2 菌丝长势测定:将18个蛹虫草菌株分别接种于PPDA培养基中,22℃恒温避光培养,待菌丝即将长满平板时,用7mm打孔器取相同半径菌块接种于PPDA培养基中央,从第4天开始采用十字划线法每隔两天测定菌丝长速,共测定16d,培养结束时观察菌落形态、颜色并记录。每个处理3个重复。
1.2.3 栽培出草试验:将活化好的菌株接种液体培养基制作液体菌种,之后接种到出草培养基上进行出草试验。用7mm打孔器取5块活化好的菌块于液体培养基中,23℃ 140r/min避光培养3-4d;取10mL液体菌种接种于大米培养基中,23℃避光培养4-5d;发菌结束后将培养基在14℃下避光培养6h进行低温刺激;最后将其转至23℃下光照培养,待子实体成熟后即可采收。
1.2.4 活性物质的提取及测定:(1)虫草素的提取及测定:参考张鑫喆等(2018)的方法并稍作调整,采用超声波热水提取法(刘春泉等2007;Zhang et al. 2012)。将虫草子实体粉碎后过80目筛,精确称取2g样品粉末,用50%的乙醇作为溶剂,以1:50的料液比80℃超声波处理20min(功率48W),80℃水浴浸提10min,重复4次。离心后取上清液,0.22μm微孔滤膜过滤后取20μL样品进行高效液相色谱检测。色谱条件为:色谱柱Venusil MP C18柱(5µm,4.6mm×250mm),流动相为水(A相)-甲醇(B相);流速1mL/min;检测波长254nm;柱温40℃;进样量20μL。洗脱程序为0-5min:A-100%,B-0%;5-10min:A-95%,B-5%;10-30min:A-70%,B-30%;30-45min:A-100%,B-0%。
(2)腺苷的提取及测定:参考张鑫喆等(2018)的方法并稍作调整,采用超声波热水提取法(刘春泉等2007;Zhang et al. 2012)。称取蛹虫草子实体粉末0.5g,加入去离子水80mL,85℃提取2h。待冷却至室温,过滤、定容、离心,0.22μm微孔滤膜过滤上清液后,取20μL样品进行高效液相色谱检测。色谱条件为:色谱柱Venusil MP C18 柱(5µm,4.6mm×250mm),流动相为甲醇(A相)-水(B相);流速1mL/min;检测波长260nm;柱温25℃;进样量20µL。洗脱程序为0-10min:A-25%,B-75%。
(3)粗多糖的提取及测定:参考李小一等(2019)、温文娟等(2020)的方法并稍作调整。采用热水-醇沉法,将虫草样品充分研磨后,过80目筛后精确称取5g样品于100mL离心管中,加入10倍体积去离子水后沸水浴加热1h。于12 000r/min离心5min,取20mL上清液于离心管中,加入3倍体积无水乙醇, 4℃过夜,离心弃上清,于50℃下烘干至恒重。采用蒽酮-硫酸法进行测定,将样品溶液浓度调整至测定范围内,精确吸取2mL置于干燥洁净的试管中,立即加入6mL蒽酮试剂,振荡混匀。所有处理样品于沸水浴中加热15min,取出后迅速浸于冰水浴中冷却15min,每个浓度3个重复。
(4)β-类胡萝卜素的提取及测定:参考刘新艳等(2017)、洪健等(2019)的方法并稍作调整,采用超声波热水-醇提法,将虫草样品充分研磨后,过80目筛后精确称取3g样品于100mL离心管中,加入20倍体积60%无水乙醇进行热水浸提。离心后取上清液,0.22µm滤膜过滤后取20μL样品进行高效液相色谱检测。色谱条件:色谱柱为Venusil MP C18 柱(5µm,4.6mm×250mm),流动相为乙腈(A相)-丙酮(B相);流速1.5mL/min;检测波长450nm;柱温30℃;进样量10μL。洗脱程序0-10min:A-95%,B-5%;10-40min:A-40%,B-60%;40-60min:A-99%,B-1%。
(5)叶黄素的提取及测定:参考李秀鑫等(2020)的方法并稍作调整。采用超声波热水-醇提法,称取1g蛹虫草子实体粉末,加入50倍体积的无水乙醇,80℃下超声波(240W)浸提2h。离心后取上清液用紫外分光光度计进行测定。将样品溶液浓度调整至指定范围内,于447nm测定吸光度值。
1.3 交配型基因的检测
参考鲍大鹏等(2017)报道的交配型基因MAT-alpha和MAT-HMG合成引物(表2)。PCR反应体系:2×Taq Master Mix 12.5μL,交配型引物各1μL,ddH2O 10.5μL,模板1μL。PCR反应条件:95℃预变性3min,95℃变性15s,60℃退火15s,72℃延伸1min,35个循环,72℃延伸5min。反应产物用1%琼脂糖凝胶电泳检测。
表2 交配型引物序列
Table 2
| 引物名称 Primer | 序列 Primer sequence (5’-3’) |
|---|---|
| MAT1-F | CGCGCAAAACGACCATTGAA |
| MAT1-R | ATATACCTTCGCGATCATTG |
| MAT2-F | ATGGATCTGCAACTGGATCGGACCA |
| MAT2-R | CTACATGATTGACTCCGGGCTCATTG |
1.4 数据分析
参考朱丽娜等(2018)的最大-最小归一化算法a=(X-Xmin)/(Xmax-Xmin),对分离自6株野生蛹虫草不同部位的菌株的菌丝长速、子实体产量和活性成分含量进行分析,综合各成分所得分值,绘制雷达图,进行品质综合评价。
本实验中数据均采用SPSS软件进行统计分析,采用单因素方差分析,P<0.05表示差异显著。
2 结果与分析
2.1 不同菌株在PPDA培养基上的菌丝长速测定和菌落形态观察
对分离得到的18个蛹虫草菌株进行菌丝长速测定和菌落形态观察(表3)。菌丝长速方面,除菌株F2-1、F4-1和F5-2长速较慢外,其余15个菌株间无显著差异;菌落形态方面,菌株F2-1、F3-3、F4-1和F5-1为绒毛状,其余菌株菌落致密;色素产生方面,菌株F1-1、F2-2、F3-1、F3-3、F4-3、F5-1、F5-2和F5-3均产生黄色色素,其余菌株不产色素。
表3 十八个蛹虫草菌株的菌丝长速和菌落特征
Table 3
| 菌株 Strains | 日均长速 Mycelial growth rate (mm/d) | 菌落特征 Characteristic of colony | 菌株 Strains | 日均长速 Mycelial growth rate (mm/d) | 菌落特征 Characteristic of colony |
|---|---|---|---|---|---|
| F1-1 | 2.028±0.048 bc | 致密、淡黄色Dense, light yellow | F4-1 | 1.222±0.048 c | 绒毛状、白色Fluffy, white |
| F1-2 | 2.417±0.289 ab | 致密、白色Dense, white | F4-2 | 2.222±0.048 abc | 致密、白色Dense, white |
| F1-3 | 2.472±0.481 ab | 致密、白色Dense, white | F4-3 | 2.306±0.127 ab | 致密、淡黄色Dense, light yellow |
| F2-1 | 1.958±0.191 bc | 绒毛状、白色Fluffy, white | F5-1 | 2.417±0.220 ab | 绒毛状、淡黄色Fluffy, light yellow |
| F2-2 | 3.222±0.419 ab | 致密、淡黄色Dense, light yellow | F5-2 | 1.694±0.127 bc | 致密、淡黄色Dense, light yellow |
| F2-3 | 3.722±0.127 a | 致密、淡黄色Dense, light yellow | F5-3 | 2.222±0.529 abc | 致密、淡黄色Dense, light yellow |
| F3-1 | 2.000±0.167 bc | 致密、淡黄色Dense, light yellow | F6-1 | 2.028±0.048 bc | 致密、白色Dense, white |
| F3-2 | 2.222±0.127 abc | 致密、白色Dense, white | F6-2 | 2.194±0.210 bc | 致密、白色Dense, white |
| F3-3 | 2.444±0.192 ab | 绒毛状、淡黄色Fluffy, light yellow | F6-3 | 2.500±0.464 ab | 致密、白色Dense, white |
注:同一列不同字母表示显著性差异(P<0.05). 下同
Note: The different letters on the same list mean significant difference (P<0.05). The same below.
2.2 栽培出草试验
对分离到的18个菌株进行出草试验(图1、图2和表4)。菌核分离得到的菌株整体出草效果较差,菌株F1-1、F2-1、F5-1仅形成少量细小的、有子囊壳的子实体,而菌株F3-1、F4-1和F6-1仅扭结形成短小的子实体,无子囊壳;子座分离菌株的整体出草效果要优于菌核分离的菌株,其中菌株F2-2、F4-2和F5-2均能正常出草且形成大量子实体,F1-2和F6-2形成少量细小的、有子囊壳的子实体,F3-2仅扭结形成短小的子实体,无子囊壳;孢子分离得到的菌株整体出草效果最好,6个菌株均能形成有子囊壳的子实体,子实体颜色更深,出草整齐,子实体数量显著优于子座和菌核部位分离的菌株;F2-3、F3-3、F6-3产量显著高于菌核和子座分离的菌株,F4-2和F4-3、F5-2和F5-3产量显著高于菌核分离的菌株,F1-1和F1-3产量显著高于F1-2,子囊孢子分离得到的菌株产量相比于菌核和子座普遍较高。
图1
图1
十八个蛹虫草菌株的出草图片
A:菌核分离;B:子座分离;C:孢子分离
Fig. 1
The morphology of fruiting bodies of 18 Cordyceps militaris strains isolated.
A: Strains isolated from sclerotium; B: Strains isolated from stroma; C: Strains isolated from spore.
图2
图2
十八个菌株子实体横切面
标尺=5mm
Fig. 2
Cross section of fruiting bodies of 18 strains.
Bar=5mm.
表4 出草菌株的生长指标统计
Table 4
| 菌株 Strains | 子实体颜色 Fruiting body color | 子囊壳密度 Perithecium density | 产量 Yield (mg) | 子实体形态 Fruiting body morphology |
|---|---|---|---|---|
| F1-1 | 淡黄色Light yellow | ++ | 4.67±0.57 a | 细短圆头 Thin, short, orbicular head |
| F1-2 | 橙黄色Orange | + | 0.70±0.70 b | 细短圆头 Thin, short, orbicular head |
| F1-3 | 橙黄色Orange | ++ | 5.70±0.50 a | 粗长圆头 Thick, long, orbicular head |
| F2-1 | 橙黄色Orange | +++ | 1.63±0.45 b | 细长圆头 Thin, long, orbicular head |
| F2-2 | 橘黄色Rich orange | +++ | 6.70±0.87 b | 粗长圆头 Thick, long, orbicular head |
| F2-3 | 橘黄色Rich orange | ++ | 15.53±1.84 a | 粗长圆头 Thick, long, orbicular head |
| F3-1 | 淡黄色Light yellow | - | 1.03±0.25 b | 细长尖头 Thin, long, sharp head |
| F3-2 | 淡黄色Light yellow | - | 1.17±0.32 b | 粗短尖头 Thick, short, sharp head |
| F3-3 | 橘黄色Rich orange | + | 13.70±1.20 a | 粗长圆头 Thick, long, orbicular head |
| F4-1 | 淡黄色Light yellow | - | 0.37±0.38 b | 粗短尖头 Thick, short, sharp head |
| F4-2 | 橘黄色Rich orange | ++ | 13.3±1.31 a | 细长尖头 Thin, long, sharp head |
| F4-3 | 橘黄色Rich orange | + | 13.43±0.70 a | 细长尖头 Thin, long, sharp head |
| F5-1 | 橙黄色Orange | + | 10.50±0.70 b | 细长尖头Thin, long, sharp head |
| F5-2 | 橘黄色Rich orange | +++ | 15.47±1.46 a | 细长尖头Thin, long, sharp head |
| F5-3 | 橘黄色Rich orange | ++ | 13.43±1.01 a | 粗长圆头Thick, long, orbicular head |
| F6-1 | 淡黄色Light yellow | - | 1.60±0.70 b | 粗短尖头Thick, short, sharp head |
| F6-2 | 橘黄色Rich orange | + | 2.87±0.31 b | 细长圆头Thin, long, orbicular head |
| F6-3 | 橘黄色Rich orange | ++ | 7.23±0.75 a | 粗长圆头Thick, long, orbicular head |
注: -:无;+:稀疏;++:浓密;+++:很浓密
Note: -: None; +: Sparsity; ++: Dense; +++: Very dense.
不同菌株间进行比较发现,F2、F4和F5的子座和孢子分离获得的菌株的出草效果较好,产量和整齐度较高,其中菌株F2-2和F2-3的子实体粗长、圆头,且颜色较深,均为橘黄色,商品性状较优良,可进一步对其进行驯化栽培。
进一步将18个菌株的出草图片与6个野生蛹虫草的子实体图片进行比较发现,孢子分离的菌株的子实体形状、大小、颜色更接近野生子实体(图3),其中菌株F2、F3和F5孢子分离菌株的子实体相比野生子实体更为粗壮、子囊壳更浓密。该结果可为优良菌种的提纯复壮提供一定的理论指导。
图3
图3
六个野生蛹虫草子实体与18个菌株中出草菌株的单个子实体图
A:菌核分离;B:子座分离;C:孢子分离;标尺=1.5cm
Fig. 3
The morphology of fruiting bodies of 6 wild and 18 isolated strains of Cordyceps militaris.
A: Strains isolated from sclerotium; B: Strains isolated from stroma; C: Strains isolated from spore. Bar=1.5cm.
2.3 活性物质测定
为进一步探究蛹虫草不同部位分离菌株的活性物质含量,对出草菌株子实体样品进行多种活性物质的测定(表5),除F1分离的3个菌株外,其他5个蛹虫草样本不同部位分离菌株的子实体中各活性成分含量都表现出相同的规律,即孢子和子座分离的菌株均显著高于菌核分离的菌株。进一步比较分析发现,18个菌株的多糖含量在14.500-131.983mg/g之间,虫草素含量在0.725-6.599mg/g之间,两种活性成分含量表现出相同的趋势,含量均以F5-2最高,F4-1最低,且分离自F4、F5和F6子座的子实体中两种物质含量均显著高于其子囊孢子和菌核部位分离的菌株,而F2和F3中则以孢子分离的子实体中含量较高;N6-(2-羟乙基)腺苷含量在0.177-0.571mg/g之间,其中以分离自F4各菌株中普遍较高,分离自F3各菌株中含量较低;β-类胡萝卜素含量在34.436-124.256μg/g之间,其中以分离自F2各菌株中普遍较高;叶黄素含量在0.094-0.397mg/g之间,其中以分离自F2的各菌株中普遍较高。
表5 出草菌株活性物质测定结果
Table 5
| 菌株 Strains | 多糖 Polysaccharides (mg/g) | 虫草素 Cordycepin (mg/g) | 腺苷 Adenosine (mg/g) | β-类胡萝卜素 β-carotene (μg/g) | 叶黄素 Xanthophyll (mg/g) |
|---|---|---|---|---|---|
| F1-1 | 71.117±1.079 a | 3.556±0.054 a | 0.263±0.008 b | 50.137±2.156 b | 0.108±0.004 b |
| F1-2 | 34.600±1.744 c | 1.730±0.087 c | 0.282±0.006 b | 41.477±0.628 c | 0.136±0.001 a |
| F1-3 | 42.367±1.150 b | 2.118±0.058 b | 0.359±0.019 a | 61.210±0.968 a | 0.131±0.012 a |
| F2-1 | 43.967±2.059 c | 2.198±0.103 c | 0.332±0.016 c | 88.889±1.413 c | 0.168±0.007 b |
| F2-2 | 47.907±0.372 b | 2.395±0.019 b | 0.423±0.009 a | 124.256±1.800 a | 0.173±0.018 b |
| F2-3 | 97.203±0.486 a | 4.860±0.024 a | 0.379±0.004 b | 93.302±2.594 b | 0.334±0.023 a |
| F3-1 | 24.300±0.625 c | 1.215±0.031 b | 0.132±0.016 b | 55.177±1.455 c | 0.200±0.028 b |
| F3-2 | 31.767±0.666 b | 1.588±0.033 b | 0.177±0.006 a | 65.105±1.679 b | 0.218±0.010 b |
| F3-3 | 51.833±2.040 a | 2.441±0.358 a | 0.197±0.003 a | 72.056±0.464 a | 0.397±0.016 a |
| F4-1 | 14.500±0.656 c | 0.725±0.033 c | 0.264±0.021 b | 44.229±1.875 b | 0.094±0.004 c |
| F4-2 | 94.133±0.569 a | 4.708±0.028 a | 0.571±0.040 a | 55.116±1.380 a | 0.137±0.001 a |
| F4-3 | 41.817±1.475 b | 2.091±0.074 b | 0.563±0.007 a | 55.255±0.591 a | 0.117±0.003 b |
| F5-1 | 45.300±1.603 c | 2.265±0.080 c | 0.123±0.003 c | 43.400±0.484 c | 0.132±0.001 b |
| F5-2 | 131.983±2.935 a | 6.599±0.147 a | 0.247±0.009 b | 52.762±1.280 b | 0.180±0.004 a |
| F5-3 | 74.900±0.608 b | 3.745±0.030 b | 0.298±0.008 a | 55.055±1.243 a | 0.126±0.009 b |
| F6-1 | 43.200±1.706 c | 2.160±0.085 c | 0.206±0.007 b | 34.436±0.490 c | 0.136±0.003 b |
| F6-2 | 114.250±1.693 a | 5.780±0.212 a | 0.444±0.017 a | 69.187±0.607 a | 0.152±0.004 b |
| F6-3 | 96.833±1.604 b | 4.642±0.415 b | 0.221±0.002 b | 64.821±2.363 b | 0.330±0.026 a |
注:不同部位分离菌株间进行差异显著性分析
Note: The significant differences between isolates from different parts were analyzed.
2.4 交配型测定
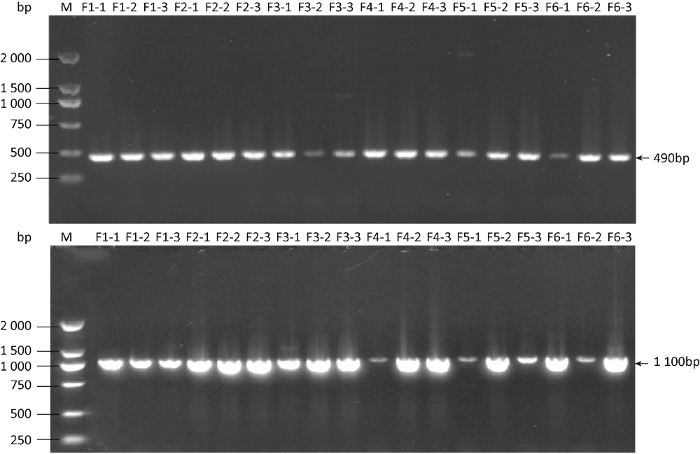
Lu et al.(2016)研究发现交配型的缺失会导致蛹虫草无法形成子实体,本实验中针对18个菌株的出草差异情况,进一步对各菌株的交配型基因进行了鉴定。经鉴定得出,18个菌株均含有交配型基因MAT-1和MAT-2(图4)。
图4
图4
交配型基因PCR扩增图谱
上图为MAT-1基因,下图为MAT-2基因;M:DL2000 marker;F1-1-F6-3:菌株
Fig. 4
PCR amplification of mating type genes of 18 strains isolated.
MAT-1 gene is shown in the upper picture, and MAT-2 gene is shown in the lower picture; M: DL2000 marker; F1-1-F6-3: Strains.
2.5 不同部位分离的蛹虫草菌株品质的综合评价
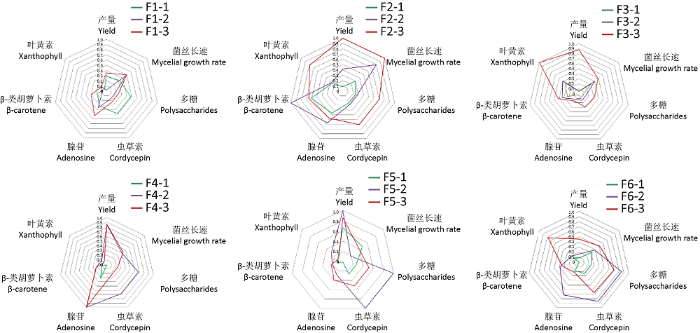
在以上各测定指标的基础上,为了更全面评价不同部位分离的菌株的综合品质,分别对分离自相同样本不同部位的蛹虫草菌株的菌丝长速、子实体产量和活性成分含量等进行归一化算法,并绘制雷达图。除F1外,其余5个样本分离的菌株中孢子和子座分离的菌株各组分均匀度均高于其菌核分离的菌株,进一步比较得出F1、F2和F3样本分离的各菌株中,孢子分离的菌株各组分均匀度均高于其子座分离的菌株(图5)。
图5
图5
不同部位分离虫草菌株品质的综合评价
Fig. 5
Comprehensive evaluation of quality of Cordyceps militaris strains isolated from different parts of wild samples.
3 讨论
本研究对分离自6株野生蛹虫草不同部位的18个菌株进行菌丝长速、菌落形态特征、出草试验和活性物质含量检测发现,不同部位分离的菌株之间以上各项测定指标均存在显著差异,其中子囊孢子分离的菌株与子座和菌核分离的菌株相比,其菌丝长速普遍较快,出草整齐且产量高;子囊孢子和子座分离菌株的子实体中活性物质含量显著高于菌核分离的菌株。进一步比较野生蛹虫草与分离菌株的子实体形态,可以看出子囊孢子分离的菌株与菌核和子座分离的菌株相比,其子实体粗壮,子囊壳浓密,更接近野生子实体。此研究结果与杨玉红等(2012)和吕延华等(2016)的研究结果较为一致,也进一步证实了子囊孢子分离法能够使子代更好地遗传亲本的优良性状这一结论,为更好地指导蛹虫草优良菌株的选育及野生菌株的驯化栽培提供了理论依据。
出草试验发现,18个菌株均可以形成子实体,其中子囊孢子分离的菌株的子实体产量普遍高于菌核和子座分离的菌株;子座分离的菌株次之;菌核分离的菌株产量最低。郑庆委等(2018)和郭尚等(2020)对于蛹虫草的菌落特征进行了研究,得出致密型菌落出草较好,绒毛状菌落不出草或出草产量低。结合出草结果,进一步对本实验出草效果不好的菌株进行菌落形态分析发现,菌落呈绒毛状的菌株(F2-1、F3-3、F4-1、F5-1)出草效果确实较差,但菌落呈致密型的菌株(F1-1、F1-2、F3-1、F3-2)也不出草或出草产量低。由此得出,菌落形态可以用于出草菌株的初步筛选,但不能作为后期出草与否的判定指标。
通过比较不同部位分离的各菌株活性物质的含量发现,虫草素、多糖、N6-(2-羟乙基)腺苷、β-类胡萝卜素和叶黄素等活性物质含量在各菌株间差异显著,但都表现出相同的规律,即子囊孢子和子座分离的菌株中各物质含量显著高于菌核分离的菌株,且在不同菌株中,虫草素和多糖的含量均表现出相同的趋势。前人关于不同部位分离菌株的研究主要集中在菌丝萌发速度、生长速度和出草性状等方面(于海洋等2017;郭尚等2020;柯轶等2021),关于不同部位分离菌株的活性成分方面未见报道。本研究发现,子囊孢子和子座分离的菌株综合性状优于菌核分离的菌株,但对子囊孢子和子座分离的菌株进行比较发现,虽然子囊孢子分离的菌株在出草实验中普遍表现较优,但在活性成分含量方面,尤其是虫草素和多糖这两种主要的活性成分,子座分离菌株普遍表现较优。蛹虫草子实体中活性成分含量受多种因素影响,如子实体大小、形状和成熟度等(孙叶等2017;刘敏祥等2018),本研究所采用的样本量较少,且各菌株间子实体大小均不一致,所以本研究中活性成分的测定结果虽有一定参考性,但可能无法作为不同菌株间特性差异的评价指标。
交配型基因是控制真菌有性生殖的关键因子,蛹虫草属于二极性异宗配合真菌,交配型位点存在两类不同源的交配型MAT-1 和MAT-2,研究发现单一交配型基因菌株无法形成子实体或子座上不产生子囊壳(Lu et al. 2016)。本实验的18个菌株虽然都可以形成子实体,但不同菌株间差异较大,且菌株F3-1、F3-2、F4-1和F6-1无子囊壳的形成。经交配型鉴定发现本实验中所有菌株均含有两种交配型基因,因此推测,除交配型基因外,子囊壳的形成还受多种因素影响,如出草时间过晚、营养供应不足或菌株分离后发生退化等,具体原因还需要进一步研究。
参考文献
Application of mating type gene molecular markers to assist affinity pairing of Cordyceps militaris
Comparative study on that growth of isolate hyphae from fruiting body tissue of Cordyceps militaris
Screening of excellent strains of Cordyceps militaris
Study on the composition and characteristics of carotenoids in Cordyceps militaris fruiting body
Review on the research progress of Cordyceps militaris breeding technology
Screening of Cordyceps militaris produced high-yield active ingredients
Study on factors affecting the stability of lutein
Recent progress on methods of extraction and separation of Cordyceps militaris polysaccharide
Research progress review on cordycepin extraction and determination methods
Comparison on the main agronomic traits of two typical Cordyceps militaris with round head or pointed head fruiting body
Pathogenic fungi of artificially cultivated Cordyceps militaris
Analysis of carotenoid content in vegetables and fruits and their products by high performance liquid chromatography
Functional convergence and divergence of mating-type genes fulfilling in Cordyceps militaris
DOI:10.1016/j.fgb.2016.01.013 URL [本文引用: 2]
The solid fermentation of Ophiocordyceps sinensis strains isolated from different parts of specimen and different generations
Research on influencing factor on yield and the main active substances of Cordyceps militaris
The effect of Cmku70 disruption on the growth and fruiting body development in Cordyceps militaris
Comparison of phenol sulfuric and anthrone sulfuric method for determination of lentinan
Study on industrial cultivation technology of Cordyceps militaris
Research on different parts of the Cordyceps military tissue isolation and continuous culture
Screening on fine Cordyceps militaris strains
Evaluation of the biological activities of four species of Cordyceps (Isaria, Beauveria) mycelial crude polysaccharides
The optimization of extraction of cordycepin from fruiting body of Cordyceps militaris (L.) Link
Comparison of determination of cordycepin and adenosine in Cordyceps militaris by HPLC with different mobile phases
Correlation analysis between nutrient composition and enzyme activity of Cordyceps militaris cultivated in different substrates
Study on hyphae growth characteristics and polysaccharide yield of Cordyceps militaris from different genetic resources genomics and applied biology
Effect of different solid media on the quality of Cordyceps militaris fruit body
Comparison of the active components in fruit bodies of different strains of Cordyceps militaris
Cmku70基因敲除对蛹虫草生长发育的影响
不同种质资源蛹虫草菌丝生长特性及其多糖产量的研究