广谱抗生素的过度依赖甚至滥用,是导致金黄色葡萄球菌Staphylococcus aureus的耐药性及耐药率逐年增大的重要原因。耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus,MRSA)是引起医院感染的最常见的多重耐药菌之一,几乎对所有的β-内酰胺类抗生素耐药,也是世界卫生组织(WHO)公布的全球公共卫生最急需解决的问题清单之一(Vanessa et al. 2020)。2017年报道了11.9万例S. aureus感染病例和约2万例死亡病例,其中的MRSA感染率和死亡占比分别为44%和20%(Chung et al. 2020)。糖肽类抗生素万古霉素被认为是治疗耐药革兰氏阳性菌感染的最终防线,随着对万古霉素耐药菌株的出现,该防线也被逐渐打破(张铃铃和陈剑云 2015)。因此,寻找有效的拮抗MRSA新型药物已是当务之急。
前期活性筛选中,我们发现一株酸模内生真菌Fusarium sp. HU0298的玉米发酵物具有很好的MRSA拮抗活性。为此,在活性跟踪的指导下采用天然产物化学方法对其中的抗菌活性物质进行了分离和分析,从中分离鉴定了具有抗MRSA活性的亚油酸,并结合GC分析和单体化合物的抗菌活性测定,初步阐明该内生真菌发酵物的抗MRSA物质基础,并对亚油酸及其类似物的抗菌活性进行了构效关系分析。
1 材料与方法
1.1 材料、试剂和仪器
1.1.1 供试菌株:内生镰刀菌Fusarium sp. HU0298由惠州学院生命科学学院徐良雄副研究员等于2018年5月分离自广东省汕头市南澳岛的滨海盐生植物酸模Rumex acetosa枝条,现保藏于惠州学院天然产物化学实验室。金黄色葡萄球菌(S. aureus ATCC6538)购于广东省微生物菌种保藏中心;耐甲氧西林金黄色葡萄球菌(MRSA 11646)由广州医科大学附属第一医院广州呼吸疾病研究所呼吸疾病国家重点实验室提供。
1.1.2 试剂:石油醚、二氯甲烷、乙酸乙酯、甲醇和丙酮等分析纯(天津市大茂化学试剂厂),色谱纯甲醇和乙腈(天津市康科德科技有限公司),柱层析硅胶(青岛基亿达硅胶试剂有限公司),薄层层析硅胶板(烟台江友硅胶开发有限公司),十四烷酸、十六烷酸、十八烷酸、二十烷酸、(9E)-十八碳-9-烯酸、亚油酸和(11Z,14Z)-二十碳-11,14-二烯酸标准品(美国斯坦福分析化学公司),硫酸链霉素和氨苄西林钠(均≥99.5%,上海麦克林生化科技有限公司)。
1.1.3 仪器:Quantum-I核磁共振波谱仪(武汉中科牛津波谱技术有限公司),SunFire C18色谱柱(10mm×250mm,Waters,美国),LC-16P制备型高效液相色谱仪、GC2010plus气相色谱仪和supelco 2560色谱柱(100m× 0.25mm×0.20μm,Shimadzu,日本)。
1.2 方法
1.2.1 菌株的发酵:Fusarium sp. HU0298的发酵采用玉米固体培养基,配方为每500mL发酵罐中含60g玉米和60mL自来水,121℃灭菌30min。将菌株接种于PDA培养基上,28℃黑暗培养3d后,挑取菌柄接种至装有30mL PDB培养基的锥形瓶内,150r/min、28℃黑暗中振荡培养2d,制备一级种子液。吸取1mL一级种子液接种至装有200mL PDB培养基的锥形瓶内,于相同条件下培养2d,制备二级种子液。吸取5mL二级种子液均匀接种至玉米培养基(约60L)中,(28±2)℃的黑暗条件下静置培养35d。
1.2.2 发酵物的提取与分离:以95%乙醇对发酵物浸提3次后过滤,滤液减压浓缩除去乙醇后用石油醚萃取。石油醚萃取物(115g)进行正相硅胶柱层析,石油醚-乙酸乙酯系统(90:10-30:70)和二氯甲烷-甲醇系统(90:10-85:15)依次梯度洗脱,经薄层层析分析合并后得到21个流分(Fr.1-Fr.21)。经活性追踪,流分Fr.2-Fr.6均具有抗MRSA活性,其中流分Fr.5和Fr.6的抗MRSA活性最为显著。因此,从流分Fr.6(7.2g)中取50mg样品,采用HPLC纯化,80%甲醇等度洗脱,得到化合物A(tR 57.8min,15.9mg)。
1.2.3 抗菌活性测试:采用滤纸片琼脂扩散法(常东东等 2012)进行,每滤纸片中活性流分和单体化合物的载样量分别为500µg和250µg,每个测试设置3个重复,抑菌圈半径为3次结果的平均值。
1.2.4 活性流分的脂肪酸组成分析:样品的甲酯化处理:称取石油醚萃取物中具抗菌活性且富含脂肪酸的Fr.2-Fr.6组分各60mg,加入4mL异辛烷和200µL氢氧化钠甲醇溶液猛烈振摇后静置至澄清,加入1.0g硫酸氢钠猛烈振摇后静置,取上清液进行后续GC分析。
脂肪酸组成的GC分析方法:流速:2.0mL/min;进样量:1μL;分流比:10:1;进样口温度:225℃;升温程序:140℃保持0.5min,5℃/min升到200℃,保持5min,1℃/min升到235℃;检测器:FID,温度为280℃。
2 结果与分析
2.1 化合物A的结构鉴定
化合物A:透明无色油状液体;1H NMR (400MHz, CDCl3) δ 5.36 (4H, m, H-9/10/12/13), 2.77 (2H, t, J= 6.6Hz, H-11), 2.35 (2H, t, J=7.1Hz, H-2), 2.04 (4H, m, H-8/14), 1.63 (2H, m, H-3), 1.32 (14H, m, H-4/5/6/7/15/16/17), 0.89 (3H, t, J=6.3Hz, H-18); 13C NMR (101MHz, CDCl3) δ 180.08 (C-1), 130.36 (C-13), 130.16 (C-9), 128.20 (C-12), 128.04 (C-10), 34.16 (C-2), 31.68 (C-16), 29.73 (C-7), 29.50 (C-15), 29.29 (C-6), 29.23 (C-4), 29.18 (C-5), 27.36 (C-8), 27.33 (C-14), 25.78 (C-11), 24.81 (C-3), 22.73 (C-17), 14.22 (C-18)。1H NMR谱显示该化合物有4个双键碳上质子信号[δ 5.35 (m, 4H)],在δ 2.77、2.35和0.89处有3个t峰,其中包括1个甲基质子信号[δ 0.89 (t, J=6.3Hz, 3H)],以及在δ 1.32处有超过15个亚甲基质子信号。13C NMR谱则显示该化合物在δ 180.0处有1个羰基碳信号,4个双键碳上信号(δ 130.3,130.1,128.2和128.0)和一个甲基碳信号δ 14.2,在δ 22.5-34.5范围内存在大量的亚甲基碳信号,说明该化合物为一个两个双键取代的长链脂肪酸。结合其ESI-MS数据并对比Kim et al.(1997)的报道,确定该化合物为亚油酸(linoleic acid)(图1)。
图1
2.2 化合物A的抗菌活性
采用滤纸片琼脂扩散法评价化合物A(亚油酸)对甲氧西林耐药和敏感的2株金黄色葡萄球菌抗菌活性,结果表明亚油酸载量为250µg时,对S. aureus ATCC6538和MRSA 11646的抑制活性明显,抑菌圈半径均为4.0mm。阳性对照中,载量为2.5µg时,硫酸链霉素对S. aureus ATCC6538和MRSA 11646的抑菌圈半径分别为2.5mm和2.0mm;而相同剂量下氨苄西林钠对S. aureus ATCC6538的抑菌圈半径为4.5mm,对MRSA 11646则未表现出明显的抑制活性。
2.3 活性流分及其主要脂肪酸成分的抗菌活性
对除亚油酸外的其他脂肪酸成分:十六烷酸、十八烷酸、二十烷酸、(9E)-十八碳-9-烯酸和(11Z,14Z)-二十碳-11,14-二烯酸进行抗菌活性评价,其中只有(11Z,14Z)-二十碳-11,14-二烯酸对S. aureus ATCC6538和MRSA 11646表现出明显的抑制效果,载量为250µg时,抑菌圈半径均为3.0mm,略小于亚油酸,而上述其余测试脂肪酸均未显示出抗菌活性。
为了比较活性流分的抗菌活性差异,探讨其中的脂肪酸类化合物的甲酯化对其抗菌活性的影响,对活性流分Fr.2-Fr.6甲酯化前后的样品进行了抗菌活性测定。载量为500µg时,流分Fr.2-Fr.6均对2株金黄色葡萄球菌表现出明显的抑菌活性,且各流分甲酯化与否均对S. aureus ATCC6538和MRSA 11646显示出几乎相同的抑菌圈半径,说明亚油酸的甲酯化不影响其发挥抗菌活性(表1)。
表1 石油醚萃取物中活性流分抗金黄色葡萄球菌的抑菌圈半径
Table 1
| 活性流分 Active fraction | 流分编号 Fractions No. | 流分编号(甲酯化) Fractions No. (methyl esterification) | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Fr.1 | Fr.2 | Fr.3 | Fr.4 | Fr.5 | Fr.6 | Fr.7 | Fr.2′ | Fr.3′ | Fr.4′ | Fr.5′ | Fr.6′ | ||
| S. aureus ATCC6538 | 0.0 | 0.0 | 1.0 | 2.0 | 2.0 | 3.0 | 0.0 | 0.0 | 1.0 | 2.0 | 2.0 | 3.0 | |
| MRSA 11646 | 0.0 | 1.0 | 1.0 | 3.0 | 3.0 | 3.0 | 0.0 | 1.0 | 1.0 | 3.0 | 3.0 | 3.0 | |
2.4 活性流分的脂肪酸组成分析
表2 石油醚萃取物中活性流分的脂肪酸成分及比例
Table 2
| 化合物 Compound | 保留时间 Retention time (min) | 峰面积 Peak area (%) | 分子式 Molecular formula | 分子量 Molecular weight | ||||
|---|---|---|---|---|---|---|---|---|
| Fr.2 | Fr.3 | Fr.4 | Fr.5 | Fr.6 | ||||
| 丁酸甲酯 Methyl butyrate | 7.7 | 0.06 | 0.99 | 4.14 | 11.11 | 3.06 | C5H10O2 | 102.13 |
| 己酸甲酯 Methyl caproate | 8.1 | 1.12 | 1.23 | 5.97 | 1.87 | 1.09 | C7H14O2 | 130.18 |
| 辛酸甲酯 Methyl octanoate | 8.9 | 0.13 | 0.10 | 0.40 | C9H18O2 | 158.24 | ||
| 十一碳酸甲酯 Methyl undecanoate | 10.6 | 0.46 | C12H24O2 | 200.32 | ||||
| 十六碳酸甲酯 Methyl hexadecanoate | 16.0 | 6.98 | 7.12 | 14.49 | 7.62 | 9.83 | C17H34O2 | 270.45 |
| (9Z)-十六碳-9-烯酸甲酯 (9Z)-methyl hexadeca-9-enoate | 17.0 | 0.06 | 0.12 | 0.31 | 0.14 | C17H32O2 | 268.43 | |
| 十七碳酸甲酯 Methyl heptadecanoate | 17.5 | 0.19 | 0.16 | C18H36O2 | 284.48 | |||
| 十八碳酸甲酯 Methyl stearate | 19.1 | 1.12 | 1.05 | 1.10 | 1.11 | 2.73 | C19H38O2 | 298.50 |
| (9E)-十八碳-9-烯酸甲酯 (9E)-methyl octadeca-9-enoate | 19.7 | 2.00 | 0.66 | C19H36O2 | 296.49 | |||
| (9Z)-十八碳-9-烯酸甲酯 (9Z)-methyl octadeca-9-enoate | 20.2 | 9.30 | 11.14 | 17.55 | 10.20 | 25.59 | C19H36O2 | 296.49 |
| (9E,12E)-十八碳-9,12-二烯酸甲酯 (9E,12E)-methyl octadeca-9,12-dienoate | 21.2 | 19.27 | 8.34 | 0.97 | 2.51 | C19H34O2 | 294.47 | |
| (9Z,12Z)-十八碳-9,12-二烯酸甲酯(亚油酸甲酯) (9Z,12Z)-methyl octadeca-9,12-dienoate (Methyl linoleate) | 22.3 | 11.93 | 27.29 | 44.50 | 51.18 | 50.75 | C19H34O2 | 294.47 |
| 二十碳酸甲酯 Methyl arachidate | 22.9 | 27.98 | 30.06 | 1.50 | 6.25 | 0.20 | C21H42O3 | 342.56 |
| (6Z,9Z,12Z)-十八碳-6,9,12-三烯酸甲酯 (6Z,9Z,12Z)-methyl octadeca-6,9,12-trienoate | 23.7 | 0.15 | C19H32O2 | 292.48 | ||||
| (9Z,12Z,15Z)-十八碳-9,12,15-三烯酸甲酯 (9Z,12Z,15Z)-methyl octadeca-9,12,15-trienoate | 24.8 | 0.14 | 0.60 | 0.24 | 2.13 | 1.68 | C19H32O2 | 292.48 |
| 二十一碳酸甲酯 Methyl heneicosanoate | 24.1 | 0.35 | 0.77 | C22H44O2 | 340.58 | |||
| (11Z,14Z)-二十碳-11,14-二烯酸甲酯 (11Z,14Z)-methyl eicosa-11,14-dienoate | 26.9 | 0.09 | C21H38O2 | 322.52 | ||||
| (13Z)-二十二碳-13-烯酸甲酯 (13Z)-methyl docosa-13-enoate | 29.1 | 0.27 | 0.34 | C23H44O2 | 352.59 | |||
| (13Z,16Z)-二十二碳-13,16-二烯酸甲酯 (13Z,16Z)-methyl docosa-13,16-dienoate | 32.3 | 0.34 | 0.53 | 0.21 | 0.53 | 0.98 | C23H42O2 | 350.58 |
| 二十四碳酸甲酯 Methyl tetracosanoate | 33.0 | 0.52 | C25H50O2 | 382.66 | ||||
| (5Z,8Z,11Z,14Z,17Z)-二十碳 -5,8,11,14,17-五烯酸甲酯 (5Z,8Z,11Z,14Z,17Z)-methyl eicosa-5,8,11,14,17-pentaenoate | 33.8 | 1.86 | 2.58 | 4.01 | 2.12 | 2.48 | C20H30O2 | 302.45 |
| (15Z)-二十四碳-15-烯酸甲酯 (15Z)-methyl tetradeca-15-enoate | 34.9 | 0.13 | 0.10 | 0.19 | C25H48O2 | 380.65 | ||
| (4Z,7Z,10Z,13Z,16Z,19Z)-二十二碳 -4,7,10,13,16,19-六烯酸甲酯 (4Z,7Z,10Z,13Z,16Z,19Z)-methyl docosa-4,7,10,13,16,19-hexaenoate | 42.3 | 0.11 | 0.40 | 0.40 | C23H34O2 | 342.51 | ||
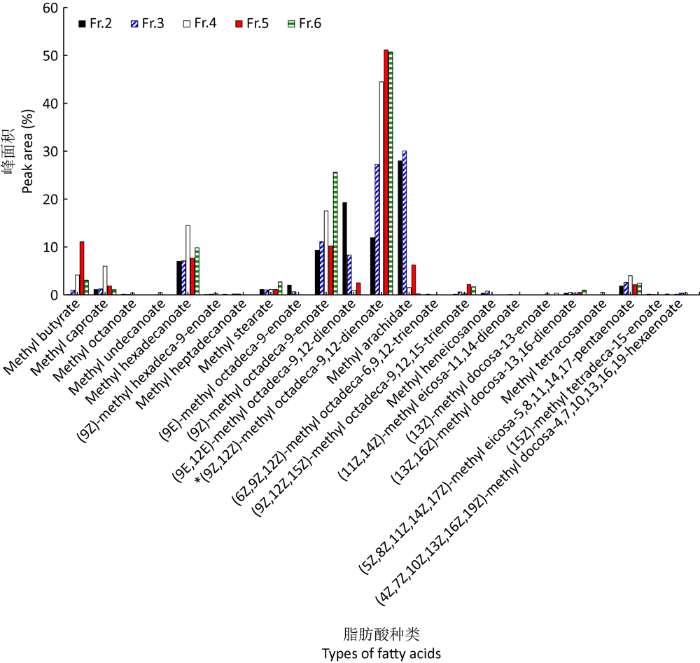
图2
图2
石油醚萃取物中活性流分的脂肪酸成分及比例(*为亚油酸甲酯)
Fig. 2
Fatty acids’ composition and proportion of the active fractions in petroleum ether extract of Fusarium sp. HU0298 (*methyl linoleate).
3 讨论
脂肪酸在自然界中分布广泛、种类丰富,具有抗炎(Panati et al. 2020)、抗肿瘤(Griffitts et al. 2010)以及抗菌(Patrica et al. 2020)等多种生物活性。近年关于植物油抗菌活性时有报道,如Ukil et al.(2019)发现黄野百合Crotalaria micans种子油具有抗金黄色葡萄球菌、枯草芽孢杆菌Bacillus subtilis、大肠杆菌Escherichia coli和铜绿假单胞菌Pseudomonas aeruginosa的活性,主要成分包括二十烷酸(37.99%)、十六烷酸(32.48%)和亚油酸(10.47%)。Asmara et al.(2019)研究指出桃花心木Swietenia mahagoni种子油对金黄色葡萄球菌表现出较强的抑制活性,并分析发现其中含有多不饱和脂酸,包括油酸(37.02%)、亚油酸(24.70%)、十六烷酸(15.49%)、十八烷酸(14.04%)、亚麻酸(7.33%)、花生酸(0.84%)、三聚氰酸(0.33%)和(9Z)-十六碳-9-烯酸(0.28%)。但上述研究均未明确是哪种脂肪酸起着主要的抗菌活性。
本研究从酸模内生镰刀菌HU0298玉米发酵物的高活性流分中分离鉴定了亚油酸,并通过GC分析了各活性流分的脂肪酸组成,发现各流分中亚油酸含量越高,抗菌活性越显著。同时通过比较亚油酸和活性流分中其他主要脂肪酸成分如十六烷酸、十八烷酸、二十烷酸和(9E)-十八碳-9-烯酸抗菌活性发现,亚油酸活性最好,(11Z,14Z)-二十碳-11,14-二烯酸较好,而测试中的其他几个脂肪酸均无明显抗菌活性。上述结果说明亚油酸在镰刀菌HU0298玉米发酵物中得率高,是主要抗菌活性成分。
前人对不同脂肪酸的抗细菌活性研究不少。如张希等(2014)研究了57种脂肪酸及其衍生物对蜡样芽孢杆菌B. cereus的抑制活性,发现碳链长为10-16的甘油单酯或碳链长大于14的不饱和脂肪酸及其甘油单酯,尤其是碳链长为18-22且双键数3个以上的多不饱和脂肪酸及其甘油单酯对蜡样芽孢杆菌B. cereus活性明显,其中二十碳五烯酸的活性最强,MIC为8μg/mL。Kabara(1984)也对不同脂肪酸的抗菌活性进行了总结,认为在抗金黄色葡萄球菌活性评价中,饱和脂肪酸中十二烷酸的活性最强,单不饱和脂肪酸中只有顺式双键的(9Z)-十六碳-9-烯酸的活性最强,且顺式双键的增加往往会使其抗菌活性增强。本研究通过分析镰刀菌HU0298发酵物中脂肪酸的化学结构和抗菌活性的关系也发现,不同脂肪酸的抗菌活性与其不饱和度和链长均密切相关,链长相同的情况下,碳链上增加顺式双键,抗菌活性进一步提升。在镰刀菌HU0298玉米发酵物中虽也检测到(9Z)-十八碳-9-烯酸、(13Z)-二十二碳-13-烯酸、(13Z,16Z)-二十二碳-13,16-二烯酸、(6Z,9Z,12Z)-十八碳-6,9,12-三烯酸、(9Z,12Z,15Z)- 十八碳-9,12,15-三烯酸、(5Z,8Z,11Z,14Z,17Z)-二十碳-5,8,11,14,17-五烯酸和(4Z,7Z,10Z,13Z, 16Z,19Z)-二十二碳-4,7,10,13,16,19-六烯酸的存在,它们可能具有一定的抗菌活性,但因含量低,对相应流分抗菌活性的贡献较小。
此外,Fr.2-Fr.6流分甲酯化前后对MRSA的抑菌圈半径相当,说明甲酯化对其抗菌作用影响不大,与赵敏(2012)在小鼠炎症模型对亚油酸和亚油酸甲酯的抗炎作用的研究结果吻合。
目前,亚油酸等长链不饱和脂肪酸被报道通过与金黄色葡萄球菌等革兰氏阳性菌体内的烯酰-ACP还原酶(FabI)以及FabI-NADPH复合物结合以抑制脂肪酸的合成从而发挥抗菌作用(Zheng et al. 2005)。FabI是催化Ⅱ型脂肪酸合成中的脂肪酸链延伸反应最后一步的限速酶,并被认为是抗菌药物开发的特异性作用靶点,其中以之为靶点开发的广谱抗菌添加剂二氯苯氧氯酚已被广泛应用于日用化学品(杨旭云 2016)。此外,脂肪酸生物安全性高,大部分已被美国FDA公证为GRAS(一般公认安全),如辛酸、十八烷酸、亚油酸等,在抗菌药物研发中具有广阔的应用前景。本研究初步揭示了其抗菌物质基础,探讨了部分脂肪酸抗菌方面的构效关系,为研发安全有效的天然抗菌药物提供了理论依据。
参考文献
Antibacterial bioactivity of n-hexane extract from mahogany (Swietenia humilis Zucc.) seed and its fatty acid compound identification
Antibacterial components from the endophytic fungus A12 of Dracaena cambodiana
Molecular interaction between methicillin-resistant Staphylococcus aureus (MRSA) and chicken breast reveals enhancement of pathogenesis and toxicity for food-borne outbreak
DOI:10.1016/j.fm.2020.103602 URL [本文引用: 1]
Non-mammalian fat-1 gene prevents neoplasia when introduced to a mouse hepatocarcinogenesis model omega-3 fatty acids prevent liver neoplasia
Antimicrobial agents derived from fatty acids
DOI:10.1007/BF02678802 URL [本文引用: 1]
A study on the constituents from the roots of Astragalus membranaceus
Electrophilic nitrated fatty acids are potential therapeutic candidates for inflammatory and fibrotic lung diseases
DOI:10.1016/j.niox.2020.06.003 URL [本文引用: 1]
Free fatty acids interfere with the DNA binding activity of the virulence regulator PrfA of Listeria monocytogenes
Emergence of community- acquired methicillin-resistant Staphylococcus aureus EMRSA-15 clone as the predominant cause of diabetic foot ulcer infections in Portugal
Exploration of fatty acid from the seed oil of Crotalaria pallida Aiton for its healthcare and antibacterial efficacy
Study on the mechanism of Enoyl-ACP reductase (FabI) with triclosan derivatives and the antibacterial mechanism
Progress of drug trerapy on methicillin-resistant Staphylococcus aureus infection
Quantitative structure activity relationship of fatty acids and their derivatives against Bacillus cereus
The research on anti-inflammation of lonoleic acid and methyllinoleate
Fatty acid synthesis is a target for antibacterial activity of unsaturated fatty acids
DOI:10.1016/j.febslet.2005.08.028 URL [本文引用: 1]