皱环球盖菇Stropharia rugosoannulata Farl. ex Murrill隶属于伞菌纲Agaricomycetes、伞菌目Agaricales、球盖菇科Strophariaceae(Hawksworth 1991)。皱环球盖菇是联合国粮农组织向发展中国家推荐栽培的食用菌之一(尚俊军等 2020),在我国食用菌中是新起之秀,根据中国食用菌协会统计,2018年和2019年我国皱环球盖菇产量比上一年分别增长了96.92%和149.99%,增长速度仅次于羊肚菌,2019年产量超过了14万吨。由于皱环球盖菇抗逆性(申进文 2014)及秸秆降解能力强(谭爱华 2018),能使大量秸秆等农林废弃物变废为宝,产生经济价值(杨顺强等 2020)和生态效益(Francesc et al. 2018;Pozdnyakova et al. 2018;白云等 2020),并且皱环球盖菇营养丰富、口感嫩滑,富含丰富的活性成分(Wu et al. 2013;Liu et al. 2020;Yan et al. 2020),具有抗氧化、抗肿瘤等药用特性(Wu et al. 2014;Wu et al. 2019;Wang et al. 2021),深受人们喜爱(Brodzinska & Lasota 1981),在我国福建、江西、辽宁、四川、新疆、青海、河南、湖北等地均有大量栽培(王建宝等 2013;沈少华等 2019)。随着皱环球盖菇栽培逐渐向着规模化与产业化发展的趋势,栽培面积逐渐扩大(Zhang et al. 2017),制约皱环球盖菇产业的主要问题也逐渐凸显出来,其中皱环球盖菇优异栽培品种短缺、品种混乱、种性退化等菌种“卡脖子”问题尤为突出(任纪帆等 2020),目前主栽品种的遗传背景不明确(鲍大鹏 2019),各地引种造成“同物异名”等现象,不利于产业的健康发展。
皱环球盖菇的栽培主要受到菌种质量、气候条件和土壤理化性质影响。由于品种混乱和种性退化问题,容易导致皱环球盖菇在生产上不稳定。菌种作为食用菌重要的基础材料(张金霞等 2011),其收集、保藏、遗传多样性评价与创新利用是遗传育种中一个重要的研究方向(边银丙 2005)。针对生产中遇到的实际问题,本研究对收集的20个主栽品种进行了ISSR分子标记的遗传多样性分析,明确其亲缘关系,同时对这些菌株的主要生物学特性,包括生长最适pH和温度范围,以及产量、菌盖颜色、菌褶颜色、菇型菇质等主要农艺性状进行研究,为皱环球盖菇育种实践提供科学基础(鲍大鹏和谢宝贵 2020),为皱环球盖菇品种选育提供优良种质和中间材料,为皱环球盖菇栽培品种选择和育种提供理论参考。
1 材料与方法
1.1 供试材料
1.1.1 菌株:供试的20株皱环球盖菇菌株由江西省农业科学院(Jiangxi Academy of Agriculture Sciences,JAAS)农业应用微生物研究所(Institute of Agricultural Applied Microbiology,IAAM)收集并保藏,保藏编号及菌株来源信息见表1。
表1 供试皱环球盖菇菌株来源及编号
Table 1
| 菌株编号 Strain | 来源 Origin | 菌株编号 Strain | 来源 Origin |
|---|---|---|---|
| Sr-01 | 浙江武义栽培场 Wuyi cultivation farm, Zhejiang | Sr-11 | 福建省农业科学院食用菌研究所 Institute of Edible Fungi, Fujian Academy of Agricultural Sciences |
| Sr-02 | 北京市农林科学院 Beijing Academy of Agriculture and Forestry Sciences | Sr-12 | 福建省农业科学院食用菌研究所 Institute of Edible Fungi, Fujian Academy of Agricultural Sciences |
| Sr-03 | 江西新余栽培场 Xinyu cultivation farm, Jiangxi | Sr-13 | 江西高安栽培场 Gao'an cultivation farm, Jiangxi |
| Sr-04 | 江西省农业科学院农业应用微生物研究所 Institute of Agricultural Applied Microbiology, Jiangxi Academy of Agricultural Sciences (IAAM, JAAS) | Sr-14 | 上海市农业科学院食用菌研究所 Institute of Edible Fungi, Shanghai Academy of Agricultural Sciences |
| Sr-05 | 江西永丰栽培场 Yongfeng cultivation farm, Jiangxi | Sr-15 | 山东省农业科学院农业资源与环境研究所 Institute of Agriculture Resources and Environment, Shandong Academy of Agriculture Sciences |
| Sr-06 | 福建古田林灯菌场 Gutian Lindeng Fungi Farm, Fujian | Sr-16 | 山东省农业科学院农业资源与环境研究所 Institute of Agriculture Resources and Environment, Shandong Academy of Agriculture Sciences |
| Sr-07 | 江西万安栽培场 Wan'an cultivation farm, Jiangxi | Sr-17 | 江西省农业科学院农业应用微生物研究所 IAAM, JAAS |
| Sr-08 | 江西省金溪县合市镇栽培场 Heshi Town cultivation farm, Jinxi County, Jiangxi | Sr-18 | 江西省农业科学院农业应用微生物研究所 IAAM, JAAS |
| Sr-09 | 江西省金溪县合市镇栽培场 Heshi Town cultivation farm, Jinxi County, Jiangxi | Sr-19 | 江西省农业科学院农业应用微生物研究所 IAAM, JAAS |
| Sr-10 | 福建省农业科学院食用菌研究所 Institute of Edible Fungi, Fujian Academy of Agricultural Sciences | Sr-20 | 江西省农业科学院农业应用微生物研究所 IAAM, JAAS |
1.1.2 供试培养基:马铃薯葡萄糖琼脂(PDA)培养基:200g马铃薯,20g葡萄糖,20g琼脂,蒸馏水定容至1 000mL,pH自然;原种袋料配方:细木屑78%,麸皮20%,石灰1%,石膏1%;出菇试验配方(3 000kg/667m2,简称3:2:1配方):50%稻草,33%木屑,17%谷壳。
表2 ISSR引物列表
Table 2
| 引物名称 Primer name | 引物序列 Primer sequence (5ʹ-3ʹ) | 引物名称 Primer name | 引物序列 Primer sequence (5ʹ-3ʹ) |
|---|---|---|---|
| P1 | TGCACACACACACAC | P15 | GTGTGTGTGTGTGTGTTA |
| P2 | GTGACACACACACAC | P16 | TGTGTGTGTGTGTGTGGA |
| P3 | GTGACGACTCTCTCTCTCT | P17 | ACACACACACACACAC |
| P4 | GGATGCACACACACACAC | P18 | ACACACACACACACACC |
| P5 | CGTGTGTGTGTGTGT | P19 | ACACACACACACACACCT |
| P6 | AGTGTGTGTGTGTGT | P20 | ACACACACACACACACCTG |
| P7 | CCAGTGGTGGTGGTG | P21 | AGCAGCAGCAGCAGCAGCG |
| P8 | GGAGTGGTGGTGGTG | P22 | AAGAAGAAGAAGAAGAAGC |
| P9 | AGAGAGAGAGAGAGAGG | P23 | GAGAGAGAGAGAGAGACT |
| P10 | GAGAGAGAGAGAGAGAC | P24 | CACGAGAGAGAGAGAGA |
| P11 | GAGAGAGAGAGAGAGAAC | P25 | GAGAGAGAGAGAGAGACC |
| P12 | AGAGAGAGAGAGAGAGGC | P26 | CACCACACACACACACA |
| P13 | TCTCTCTCTCTCTCTCCG | P27 | GTATGTATGTATGTATGG |
| P14 | ACACACACACACACACCG | P28 | GTATGTATGTATGTATGC |
1.2 遗传多样性分析
将保存的皱环球盖菇菌株接于PDA培养基活化10d,接入铺了灭菌玻璃纸的平皿PDA培养基上,25℃黑暗培养10d。用无菌镊子将菌丝轻轻刮入1.5mL离心管中,称重备用。采用植物基因组DNA提取试剂盒(离心柱型 DP305)提取菌丝基因组DNA。
遗传多样性分析采用ISSR标记进行(黄晨阳等 2009),先选择两个彼此有明显拮抗菌株的5个DNA样品对28条ISSR引物进行筛选,琼脂糖凝胶电泳检测,选出电泳条带清晰、重复性好且多态性高的引物进行所有菌株的PCR扩增。
PCR扩增反应体系(20μL):含有Premix Taq 10μL,4μmol/L引物,20ng模板DNA,加灭菌双蒸水至20μL。按照上述比例将反应液依次加入0.2mL离心管中,混匀,放入PCR仪中,进行PCR扩增。反应程序:94℃预变性3min,94℃变性30s,55℃复性45s,72℃延伸2min,共35个循环,72℃延伸5min,4℃保存。PCR产物在1.5%琼脂糖凝胶电泳检测。统计各ISSR引物扩增结果,电泳条带按0/1进行2进制数据转换,条带清晰且再现性强的条带记为1,无条带的记为0,采用NTsys-pc2.10e软件绘制UPGMA系统进化树。
1.3 供试菌株生长最适pH值范围
使用1mol/L盐酸和1mol/L氢氧化钠将灭菌的PDA培养基pH分别调到4.0、5.0、6.0、7.0、8.0、9.0和10.0,将供试菌株用直径9mm打孔器打孔后接种到不同pH值的PDA培养基上,接种后置于25℃培养箱中黑暗培养,第3天开始每天测量一次菌落直径,观察与记录菌丝生长情况,每个处理设3个重复。
1.4 供试菌株最适生长温度
PDA培养基接种不同供试菌株后分别置于5、10、15、20、25、30和35℃的恒温培养箱进行黑暗培养,第3天开始每天测量一次菌落直径,观察与记录菌丝生长情况,每个处理设3个重复。
1.5 供试菌株袋料生长速度试验
将原种袋料配方混合均匀,调节含水量为60%左右,采用12cm×24cm聚丙烯折角塑料袋,每袋装干料重为150g,高温高压(121℃、0.1MPa)灭菌2.5h,自然冷却后接种,然后置于25℃恒温培养室内黑暗培养,待菌丝封料面之后,每1个星期测量并记录一次菌丝在培养料中的生长距离,每个处理3个重复。
1.6 皱环球盖菇菌株出菇试验
选用稻草、木屑和谷壳3:2:1的常用栽培配方进行20株皱环球盖菇菌株出菇试验,栽培料干重为7.5kg/m2,栽培方法见魏云辉等(2020)制定的皱环球盖菇大田栽培技术规程。试验地点在江西省农业科学院院内食用菌温室大棚内,试验采用小区设计,每个小区2.52m2,垄长4.2m,垄宽0.6m,两垄间距0.4m,各栽培料重复3次。
1.7 产量和农艺性状的测定
选取皱环球盖菇子实体菌褶未破裂菌盖呈钟形时随机统计农艺性状,产量为每个试验小区从开始出菇到出菇结束的鲜菇总重。子实体的高度、菌盖厚度、菌盖直径(十字法测量,取平均值)、菌柄长度、菌柄直径(十字法测量,取平均值)等采用游标卡尺进行测量,单菇重采用电子秤进行测量,菇体硬度采用手捏判断。菌盖直径与菌柄长度的比值为菇型比例,子实体鲜重与栽培料干重的比值为生物学效率。
2 结果与分析
2.1 ISSR分子标记分析
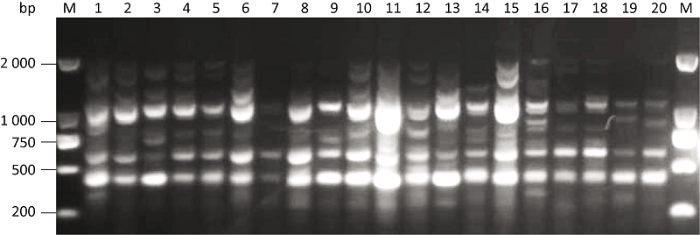
从28个食用菌通用ISSR引物中筛选出22个适宜引物,对20株供试菌株共扩增出132个条带,其中P25和P11引物扩增最多,有8个条带,P5引物扩增最少,只有4个条带。统计多态性条带结果发现,共扩增出110个多态性条带,多态性比率达到83.33%。扩增出的DNA片段条带的大小在250-2 000bp之间,图1为引物P14对20个供试菌株的扩增结果。
图1
图1
引物P14的PCR扩增图谱
Fig. 1
PCR amplification map of primer P14. M: DNA markers; 1-20: Stropharia rugosoannulata test strains Sr-01-Sr-20.
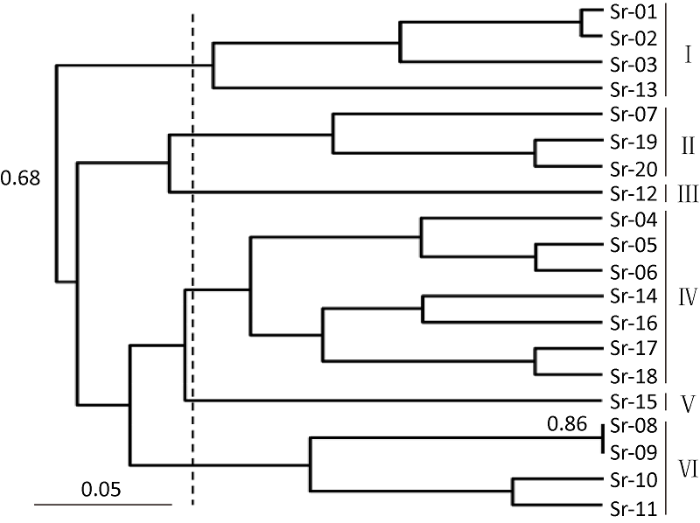
根据皱环球盖菇ISSR聚类图,20株皱环球盖菇菌株遗传相似性水平在0.68-0.86之间,在遗传相似性水平为0.72时供试菌株可分为6个类群(图2),类群Ⅰ包括4个菌株(Sr-01、Sr-02、Sr-03、Sr-13),类群Ⅱ包括3个菌株(Sr-07、Sr-19、Sr-20),类群Ⅲ包括1个菌株(Sr-12),类群Ⅳ包括7个菌株(Sr-04、Sr-05、Sr-06、Sr-14、Sr-16、Sr-17、Sr-18),类群Ⅴ包括1个菌株(Sr-15),类群Ⅵ包括4个菌株(Sr-08、Sr-09、Sr-10、Sr-11);20株皱环球盖菇菌株中Sr-12和Sr-15与其他类群的遗传差异较大;Sr-08和Sr-09遗传相似水平最高为0.86。
图2
图2
20株皱环球盖菇菌株基于ISSR分子标记分析的聚类图
Fig. 2
Cluster diagram of 20 Stropharia rugosoannulata strains based on ISSR. 1-20: Stropharia rugosoannulata test strains Sr-01-Sr-20.
2.2 皱环球盖菇菌丝生长最适pH值范围
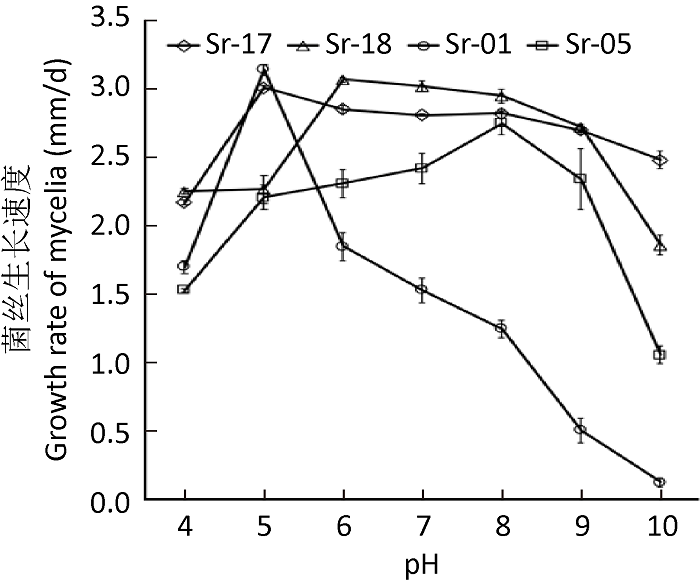
将20株供试皱环球盖菇菌株在pH值为4.0-10.0之间的PDA培养基上培养后发现所有菌株在pH 4.0-10.0之间均可生长,按照菌株在不同pH值下生长速度的适应性,可以分为4组(表3),总体表现为耐酸性的菌株有18个,但其最适pH值并不相同,最适pH值为5.0的菌株有14株,表现为在pH 5.0时生长速度最快,pH值6.0-10.0时生长速度逐渐降低,代表菌株为Sr-17;最适pH为6.0的菌株有4个(Sr-07、Sr-08、Sr-11、Sr-18);另外菌株Sr-01和Sr-14虽然最适pH也为5.0,但在高于5.0的pH值下,生长速度受到较大抑制,表现出对pH的高度敏感。2个菌株(Sr-03和Sr-05)生长最佳pH是8.0,表现出耐碱不耐酸的特性。4个类型标准菌株在各pH值下的生长速度见图3,对pH值适应性最强的菌株为Sr-17和Sr-18,在不同pH下生长速度均高于2mm/d以上,最适pH值下生长速度均在3mm/d以上,其中耐酸性最强的菌株是Sr-18,耐碱性最强的菌株是Sr-17;生长速度最快的是Sr-01,在pH 5.0条件下达到(3.14±0.04)mm/d,生长速度最慢的是Sr-01在pH 10.0条件下的(0.13±0.03)mm/d。另外,在各pH条件下总体生长最慢的菌株为Sr-15,生长速度均低于1mm/d。筛选出两株对酸碱性抗逆较强的菌株Sr-17和Sr-18。
表3 供试皱环球盖菇在PDA培养基上对pH值的适应性分组及代表菌株
Table 3
| pH值适应性 pH adaptability | 菌株 Strains | 代表菌株 Representative strain |
|---|---|---|
| 耐酸性,pH 5.0最适 Acid resistance, optimal pH 5.0 | Sr-17, Sr-04, Sr-19, Sr-10, Sr-13, Sr-02, Sr-12, Sr-16, Sr-06, Sr-09, Sr-20, Sr-15, Sr-01, Sr-14 | Sr-17 |
| 耐酸性,pH 6.0最适 Acid resistance, optimal pH 6.0 | Sr-18, Sr-07, Sr-11, Sr-08 | Sr-18 |
| 耐酸性,对pH敏感 Acid resistance, sensitive to pH | Sr-01, Sr-14 | Sr-01 |
| 耐碱性,pH8.0最适 Alkali resistance, optimal pH 8.0 | Sr-05, Sr-03 | Sr-05 |
图3
图3
培养基pH对皱环球盖菇菌丝生长速度的影响
Fig. 3
Effects of medium pH on the growth rate of Stropharia rugosoannulata mycelium.
2.3 温度对皱环球盖菇菌丝生长的影响
20株皱环球盖菇菌丝在温度5-30℃之间均可生长,最适生长温度在25-30℃。温度为5℃时,菌丝能缓慢生长,生长速度均在0.30mm/d以下。将20个菌株在5-30℃间的生长速度进行线性回归分析,菌株Sr-01、Sr-08、Sr-11、Sr-14和Sr-15在30℃时受到抑制,其回归系数较低,生长速度与温度间不符合线性关系,其余15个菌株的线性回归分析见表4,回归系数(R2)在0.949-0.989之间,菌株按照斜率即长速随温度的增长速度高低进行排列,斜率值在0.079-0.115之间。温度为35℃时,只有Sr-04、Sr-07、Sr-10、Sr-16和Sr-17这5个菌株可以萌发,且培养20d后仍具有活性,其余菌株不萌发,20d后无活性。
表4 菌株生长速度与温度间的线性回归分析
Table 4
| 菌株 Strains | 回归系数 Regression coefficients | 线性回归方程 Linear regression equation | 菌株 Strains | 回归系数 Regression coefficients | 线性回归方程 Linear regression equation |
|---|---|---|---|---|---|
| Sr-13 | 0.981 | y=0.115x-0.329 | Sr-07 | 0.979 | y=0.101x-0.161 |
| Sr-17 | 0.984 | y=0.114x-0.304 | Sr-18 | 0.976 | y=0.101x-0.155 |
| Sr-02 | 0.960 | y=0.113x-0.168 | Sr-03 | 0.949 | y=0.100x-0.066 |
| Sr-12 | 0.969 | y=0.111x-0.343 | Sr-06 | 0.976 | y=0.099x-0.198 |
| Sr-19 | 0.953 | y=0.108x-0.424 | Sr-09 | 0.972 | y=0.098x-0.079 |
| Sr-16 | 0.978 | y=0.105x-0.218 | Sr-05 | 0.987 | y=0.098x-0.210 |
| Sr-10 | 0.953 | y=0.103x-0.131 | Sr-20 | 0.989 | y=0.079x-0.164 |
| Sr-04 | 0.975 | y=0.102x-0.152 |
2.4 培养料中菌丝生长速度比较
皱环球盖菇菌丝在以木屑为主的原种袋料中均可生长,但生长速度较慢,其中生长速度最快的菌株依次是Sr-07、Sr-17、Sr-18、Sr-16和Sr-03(表5),分别为(1.20±0.09)、(1.08±0.14)、(1.02±0.01)、(1.02±0.04)和(1.02± 0.09) mm/d,其余菌株生长速度均在1mm/d以下,Sr-04生长速度最慢为0.73mm/d。
表5 皱环球盖菇菌丝吃料能力
Table 5
| 菌株 Strains | 菌丝生长速度 Mycelial growth rate (mm/d) | 菌株 Strains | 菌丝生长速度 Mycelial growth rate (mm/d) |
|---|---|---|---|
| Sr-07 | 1.20±0.09a | Sr-13 | 0.92±0.06cdef |
| Sr-17 | 1.08±0.14ab | Sr-01 | 0.91±0.09cdef |
| Sr-18 | 1.02±0.01bc | Sr-10 | 0.90±0.03defg |
| Sr-16 | 1.02±0.04bc | Sr-06 | 0.90±0.06cdef |
| Sr-03 | 1.02±0.09bc | Sr-09 | 0.85±0bcd |
| Sr-12 | 0.98±0.07bcd | Sr-11 | 0.84±0.11cdef |
| Sr-08 | 0.98±0.08 bcd | Sr-14 | 0.81±0.05efg |
| Sr-05 | 0.97±0.05bcde | Sr-15 | 0.76±0.12fg |
| Sr-02 | 0.96±0.07bcde | Sr-19 | 0.77±0.12fg |
| Sr-20 | 0.96±0.08bcde | Sr-04 | 0.73±0.12g |
注:数据为3次试验平均值±标准误差,小写英文字母表示P<0.05的差异显著性,下同
Note: Values represent the mean of three replicates ± SD; different lower case letters indicate a significant difference at P<0.05, the same below.
2.5 不同菌株产量与子实体性状比较
20株皱环球盖菇菌株出菇试验产量结果见表6,Sr-12菌株产量显著高于其他菌株,其生物学效率高达98.09%,Sr-15产量最低,生物学效率仅为3.2%,筛选出产量最高的优异菌株Sr-12。出菇时间最短的菌株为Sr-06,最长的为Sr-15。采收持续时间最长的Sr-06,最短的为Sr-15。
表6 不同菌株产量统计
Table 6
| 菌株 Strains | 单位面积产量 Yield per unit area (kg/m2) | 接种至出菇时间 Cultivation cycle from inoculation to fruiting (d) | 采收持续时间 Harvest duration (d) | 生物学效率 Biological efficiency (%) |
|---|---|---|---|---|
| Sr-01 | 3.22±0.21i | 127 | 74 | 42.89±2.74i |
| Sr-02 | 4.57±0.06fg | 110 | 73 | 60.89±0.74fg |
| Sr-03 | 4.52±0.09fg | 96 | 76 | 60.27±1.14fg |
| Sr-04 | 6.75±0.16b | 94 | 86 | 89.96±2.09b |
| Sr-05 | 5.73±0.22cd | 108 | 82 | 76.44±2.94cd |
| Sr-06 | 5.78±0.08cd | 77 | 113 | 77.11±1.07cd |
| Sr-07 | 3.94±0.40h | 112 | 80 | 52.49±5.29h |
| Sr-08 | 6.11±0.27c | 86 | 114 | 81.42±3.57c |
| Sr-09 | 4.53±0.30fg | 96 | 84 | 60.35±3.96fg |
| Sr-10 | 5.97±0.27cd | 92 | 105 | 79.55±3.61c |
| Sr-11 | 1.49±0.42j | 137 | 47 | 19.82±5.54j |
| Sr-12 | 7.36±0.34a | 94 | 86 | 98.09±4.53a |
| Sr-13 | 5.80±0.24cd | 84 | 111 | 77.38±3.2cd |
| Sr-14 | 5.93±0.2cd | 132 | 54 | 79.11±2.67c |
| Sr-15 | 0.24±0.10k | 142 | 5 | 3.2±1.27k |
| Sr-16 | 5.80±0.18cd | 108 | 79 | 77.29±2.35cd |
| Sr-17 | 4.23±0.19gh | 113 | 79 | 56.36±2.57gh |
| Sr-18 | 5.59±0.35d | 94 | 83 | 71.16±10.26de |
| Sr-19 | 4.92±0.10ef | 94 | 86 | 65.65±1.28ef |
| Sr-20 | 5.11±0.43e | 94 | 86 | 68.09±5.74e |
20株皱环球盖菇菌株子实体的农艺性状见表7,Sr-16菌株子实体个体较大,其子实体高度、菇盖直径、菇盖厚度、菇柄长和单菇重等指标均显著高于其他菌株,筛选出菇体较大、产量较好的菌株Sr-16。Sr-08和Sr-12菇体硬度较好,Sr-11和Sr-15菇体硬度较差,其他菌株菇体硬度正常。菌盖颜色大部分为酒红色(图4A),其中Sr-08菌盖颜色为淡黄色(图4B),Sr-12菌盖周围为酒红色,菌盖中心凸起部分为黄色(图4C)。菌褶颜色除菌株Sr-19为纯白色(图5C)和Sr-20为灰白色(图5B)外,其余均表现出灰黑色(图5A),而且菌褶颜色越浅,产孢量越少(图5)。纯白色菌褶的菌株菌盖颜色比灰黑色或灰白色菌褶的菌株菌盖颜色要浅(图6)。20株菌株的菇型比例(钟雪美等 1990)有19株达到优良,1株Sr-09为较好,其中Sr-12菌株菇型比例最好,达1.36。筛选出菌盖颜色和菌褶颜色显著差异的菌株Sr-08、Sr-19和Sr-20。
图4
图5
图5
灰黑、灰白和纯白色菌褶及其孢子印
Fig. 5
Grayish black, greyish white and pure white gills of Stropharia rugosoannulata and their spore print.
图6
3 讨论
本研究主要对来自本实验室选育、收集和保藏的20个皱环球盖菇菌株进行了遗传多样性分析、并检测了这些菌株的主要生物学特性和农艺性状。本研究采用ISSR标记进行菌株间的遗传多样性研究,同样采用UPGMA聚类分析,相似系数总体上较朱静娴等(2018)采用SRAP标记的要小,表现出更大的遗传差异。推测一方面是本试验所使用的群体来源更为多样,另一方面是ISSR标记的多态性更为丰富,但ISSR标记的结果不易统计,存在一定的统计误差。采用结果更加稳定、易于统计,以及基因组覆盖率更高的分子标记如SSR、SNP、InDel等标记将有助于减少误差。
皱环球盖菇菌株在pH值为4.0-10.0之间均可生长(颜淑婉 2002;萨仁图雅和图力古尔 2005),本研究有18个菌株最佳pH生长条件偏酸性,2个菌株偏弱碱性,与孙萌等(2013)的相关研究结果相近,本研究采用PDA培养基进行不同pH适应性的结果较金银慧(2020)在土壤中检测的最适pH值范围更广,可能存在菌株上的差异。皱环球盖菇菌株在温度5-30℃之间均可生长(闫培生等 2001;刘本洪 2004),最适生长温度在25-30℃(Zhou et al. 2010),其中筛选出5个菌株(Sr-04、Sr-07、Sr-10、Sr-16和Sr-17)在35℃培养20d仍具活性,比俞志纯(1996)研究的菌株具有更强的耐热性。
本试验的20个供试菌株中,Sr-12和Sr-15与其他菌株的遗传差异较大,Sr-12产量显著高于其他菌株,菇型比例最大,为1.36,菇体硬度也较好;而Sr-15产量最低、菇体硬度较差,性状表现差异较大;Sr-04和Sr-12生物学效率较高分别为89.96%与98.09%,而其他菌株的生物学效率普遍分布于60%-80%,其中Sr-04位于类群Ⅳ中,Sr-12位于类群Ⅲ,它们与同一类群菌株的生物学效率差距较大;Sr-17和Sr-18同为第Ⅳ大类,这2个菌株对不同pH值的适应性均较强,但同为Ⅳ大类的菌株Sr-05却表现为pH 8.0最适;Sr-19和Sr-20同为第Ⅱ大类,这两者菌褶颜色极其相近,并且有异于其他菌株,但同为第Ⅱ大类的菌株Sr-07却与大部分菌株比较相似;Sr-08与Sr-09、Sr-10、Sr-11同为第Ⅵ类,但Sr-08菌盖颜色显著差异于其他3个菌株;Sr-01与Sr-02、Sr-03、Sr-13同为第Ⅰ类,但只有Sr-01在温型试验中不符合线性关系。本研究的遗传多样性差异与菌株农艺性状间存在较大差异,说明皱环球盖菇种质类型丰富,性状表现多样,单纯依靠形态特征鉴定会存在一定偏差,皱环球盖菇可能同其他类型的大型真菌一样,其大多数重要的生物学特性和农艺性状都是由多个数量基因座位和栽培外在环境因素共同控制的(Gong et al. 2019)。
通过对20个供试菌株的筛选,Sr-16菌株子实体个体较大,耐高温,吃料能力较强;Sr-08菇体硬度较好,菌盖颜色为淡黄色且产量较高,Sr-12菌盖中心凸起部分红黄色且产量最高;Sr-19和Sr-20菌褶颜色为特异的纯白色和灰白色,而且菌褶颜色越浅,产孢量越少,纯白色菌褶的菌株几乎不产孢;菌株Sr-17和Sr-18耐酸性最强,耐高温以及袋料吃料能力强。这7个菌株在主要生物学特性、农艺性状和遗传多样性中差异较大,并且栽培表现优异,可作为以强抗逆性、不同菌盖颜色和不同菌褶颜色为目标的皱环球盖菇品种选育的亲本及其育种的中间材料,可为皱环球盖菇遗传多样性研究和遗传育种亲本的选择提供了理论依据。
参考文献
Effects of rice straw pretreatment and returning on soil nutrient leaching and COD
Research progress on the mating-typing locus structures of basidiomycete mushrooms
Some research directions worthy of attention in the genetics of edible mushrooms in China
Discussion on the quality of edible mushroom spawn and its management countermeasures-technical support for quality management of edible mushroom spawn in China
Chemical composition of cultivated mushrooms Part I. Stropharia rugosoannulata Farlow ex Murr
Stropharia rugosoannulata and Gymnopilus luteofolius: promising fungal species for pharmaceutical biodegradation in contaminated water
DOI:10.1016/j.jenvman.2017.07.052 URL [本文引用: 1]
High yield cultivation technique of Stropharia rugosoannulata
A resequencing-based ultradense genetic map of Hericium erinaceus for anchoring genome sequences and identifying genetic loci associated with monokaryon growth
DOI:10.3389/fmicb.2019.03129 URL [本文引用: 1]
The fungal dimension of biodiversity: magnitude, significance, and conservation
DOI:10.1016/S0953-7562(09)80810-1 URL [本文引用: 1]
Verification of genuineness for edible mushroom spawn- ISSR
Studies on the biological characteristics of Stropharia rugosoannulata
Selection of Stropharia rugosoannulata strain for decomposition of crop residues and its application in mushroom production
Isolation, characterization and antioxidant of polysaccharides from Stropharia rugosoannulata
DOI:10.1016/j.ijbiomac.2019.11.045 URL [本文引用: 1]
The degradative activity and adaptation potential of the litter-decomposing fungus Stropharia rugosoannulata
DOI:10.1007/s11274-017-2385-4 URL [本文引用: 1]
Breeding of Stropharia rugosoannulata “Shannongqiugai No. 3”
Advances in the study on Stropharia rugosoannulata
Analyses of mating systems in Stropharia rugosoannulata based on genomic data
Edible fungus production technology
A preliminary study on cultivation techniques of Stropharia rugosoannulata in northern Jiangxi
The biological characteristics of Stropharia rugosoannulata mycelia
Key points of cultivation of Stropharia rugosoannulata with crop straw
Key technical points of interplanting Stropharia rugosoannulata under forest in northern Xinjiang
Effects of drying on the structural characteristics and antioxidant activities of polysaccharides from Stropharia rugosoannulata
Technical regulation for field cultivation of Stropharia rugosoannulata
Resource diversity of Chinese macrofungi: edible, medicinal and poisonous species
DOI:10.1007/s13225-019-00432-7 URL [本文引用: 1]
Functional-food constituents in the fruiting bodies of Stropharia rugosoannulata
An unusual sterol from the mushroom Stropharia rugosoannulata
DOI:10.1016/j.tetlet.2013.06.142 URL [本文引用: 1]
Effects of nutrients and environmental factors on the mycelial growth of Stropharia rugosoannulata
Biological characteristics of Stropharia rugosoannulata
Agronomic character analysis of Stropharia rugosoannulata cultivated in solar greenhouse with different formulas and preparation techniques
Effect of cultivation of different edible fungi under grapevines
Key technology of artificial cultivation of Stropharia rugosoannulata
Chinese edible mushroom spawn
Citrus stand ages regulate the fraction alteration of soil organic carbon under a citrus/Stropharua rugodoannulata intercropping system in the Three Gorges Reservoir area, China
DOI:10.1007/s11356-017-9269-x
PMID:28639022
[本文引用: 1]

Soil carbon fractionation is a valuable indicator in assessing stabilization of soil organic matter and soil quality. However, limited studies have addressed how different vegetation stand ages under intercropping agroforestry systems, could affect organic carbon (OC) accumulation in bulk soil and its physical fractions. A field study thus investigated the impact of citrus plantation age (15-, 25-, and 45-year citrus) on the bulk soil organic carbon (SOC) and SOC fractions and yields of Stropharia rugoso-annulata (SRA) in the Three Gorges Reservoir area, Chongqing, China. Results indicated that the intercropping practice of SRA with citrus significantly increased the SOC by 57.4-61.6% in topsoil (0-10 cm) and by 24.8-39.9% in subsoil (10-30 cm). With a significantly higher enhancement under the 25-year citrus stand than the other two stands, all these citrus stands of three ages also resulted in a significant increase of free particulate OC (fPOC, 60.1-62.4% in topsoil and 34.8-46.7% in subsoil), intra-micro aggregate particulate OC (iPOC, 167.6-206.0% in topsoil and 2.77-61.09% in subsoil), and mineral-associated OC (MOC, 43.6-46.5% in topsoil and 26.0-51.5% in subsoil). However, there were no significant differences in yields of SRA under three citrus stands. Our results demonstrated that citrus stand ages did play an important role in soil carbon sequestration and fractionation under a citrus/SRA intercropping system, which could therefore provide a sustainable agroforestry system to enhance concurrently the SOC accumulation while mitigating farmland CO emission.
Comprehensive evaluation of production properties of different strains of Pleurotus ostreatus
Statistical optimization of cultivation conditions for exopolysacchride production and mycelia growth by Stropharia rugosoannulata
DOI:10.1007/s13213-009-0006-7 URL [本文引用: 1]
Genetic diversity and phylogenetic relationship analysis of 23 Stropharia rugosoannulata strains based on SRAP molecular marker
基于基因组数据解析大球盖菇交配型系统